新一代多靶点激酶抑制剂--伏罗尼布
-

-
专家 王东兴副主任药师解放军总医院医疗保障中心药剂科副主任
伏罗尼布 (CM082,vorolanib) 是具有全新化学结构的新一代多靶点酪氨酸激酶受体抑制剂。它针对血管内皮生长因子受体 (Vascular endothelial growth factor receptor, VEGFR)、血小板衍生生长因子受体 (Platelet-derived growth factor receptors,PDGFR)、c – Kit 原癌基因 (c-kitproto-oncogeneprotein ,c-Kit)、类 Fms 酪氨酸激酶-3 (Fms-like TyrosineKinase-3,Flt-3)、集落刺激因子 1 受体 (Colony-stimulating factor 1 receptor,CSF1R) 等多个靶点。这些靶点中除 c-Kit 具有阻断酪氨酸蛋白激酶 kit 受体的功能,从而抑制肿瘤的形成外,其他靶点均具有抗血管生成的作用。而且伏罗尼布能够满足靶点的特殊 PK/PD 要求,达到保留活性,降低毒性的目的,从而抑制肿瘤血管生成及肿瘤生长,拟用于晚期肾癌、结肠直肠癌、胰腺癌、黑色素瘤、白血病、胃肠道间质瘤或其他晚期实体恶性肿瘤等多种癌症的治疗。
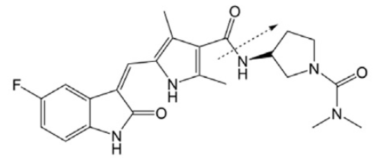
伏罗尼布的化学结构式
一.伏罗尼布片剂
2022 年 1 月 11 日,伏罗尼布片的上市许可申请获得 CDE 受理,适应症为晚期肾癌,拟用于与依维莫司联合治疗既往接受过抗血管酪氨酸激酶抑制剂治疗失败的晚期肾细胞癌患者。目前国内已批准用于晚期肾细胞癌治疗的药物包括培唑帕尼、舒尼替尼、阿昔替尼、索拉非尼、依维莫司、白介素-2、α干扰素等。但目前尚无治疗肾癌的国产创新药物上市,伏罗尼布或将成为中国第一个用于治疗晚期肾癌的国产 1 类新药,填补国内空白。
晚期肾癌的治疗以抗血管靶向药物治疗为主,但随着纳武利尤单抗为代表的免疫治疗批准用于晚期肾癌二线治疗以后,免疫与免疫药物的联合以及免疫与靶向药物的联合,包括程序性死亡蛋白-1 (programmed death-1,PD-1) /程序性死亡蛋白配体-1 (programmed death ligand-1,PD-L1) 抑制剂与细胞毒性 T 淋巴细胞相关抗原-4 抑制剂联合、免疫检查点抑制剂与靶向药物的联合,已经成为晚期肾癌临床研究的发展方向。
在一项名为 CONCEPT 的 Ⅱ/Ⅲ 期临床研究中,伏罗尼布+依维莫司联合治疗组治疗晚期肾癌患者的中位无进展生存期 (PFS) 长于依维莫司单药组 (10.0个月 vs 6.4个月)。133例接受伏罗尼布+依维莫司联合治疗的患者中,33例 (24.8%) 获得客观反应,该数据在伏罗尼布单药组与依维莫司单药组分别为 14 例 (10.5%) 和 11 例 (8.3%)。此外,联合治疗组的疾病控制率 (DCR) 也显著优于依维莫司单药组 (84.2% vs 74.4%)。
伏罗尼布片的上市许可申请获得CDE受理已经有半年时间,我们期待伏罗尼布片早日获批上市,造福于晚期肾癌患者。
二.伏罗尼布注射剂
伏罗尼布被开发用于局部给药的眼科适应症,包括湿性年龄相关性黄斑变性 (w-AMD)、糖尿病视网膜病变 (DR) 和视网膜静脉阻塞 (RVO)。湿性年龄相关性黄斑变性 (w-AMD) 是一种潜在致盲性疾病,是 60 岁及以上人群致盲的首要原因,患者通常需要每月进行一次眼部注射治疗。
伏罗尼布 (CM082) 缓释制剂 EYP-1901 是将伏罗尼布和 Durasert® 技术相结合,形成了一种新的治疗方案,可在门诊办公室注射治疗,EYP1901可生物降解,并且可以实现至少 6 个月的药物释放,有望为严重眼科疾病患者提供一种新的局部注射治疗方案。EyePoint 的 Durasert® 技术是一种已批准上市的玻璃体内给药系统,它将另一种药物注射进入玻璃体内后缓释,有效期可长达 3 年。
2021 年 11 月和 2022 年 2 月,EYP-1901 治疗 w-AMD 的 I 期临床试验中期数据公布。结果显示,其治疗具有稳定的视力和 OCT 检查结果,没有眼部或药物相关的全身性 SAE 报告,也没有剂量限制性毒性。此外,在单剂 EYP-1901 治疗之后,分别有 53% 和 41% 的病人眼睛在长达 6 个月和 9 个月内不需要任何补充抗 VEGF 注射。
三、伏罗尼布PK/PD
I期临床试验数据显示,伏罗尼布 400mg 单剂量口服给药的 T1/2 为 10.6h,Tmax 为 2.97h,Cmax 为 852ng/mL,AUC 为 7050h* ng/mL,CL/F为35.6L/h。截止到目前,伏罗尼布既有一个口服剂型获得上市许可申请的受理,又在进行眼科局部注射给药的临床研究,这一国内首创的具有全新化学结构的新一代多靶点激酶抑制剂颇具前景。
参考文献:
[1]周莉,盛锡楠.晚期肾癌的治疗规范——《CSCO肾癌诊疗指南2020》解读[J].肿瘤综合治疗电子杂志,2020,6(04):1-6+111.
[2]朱刚,刘圣杰.2020版欧洲泌尿外科学会(EAU)肾癌诊疗指南更新解读[J].中华腔镜泌尿外科杂志(电子版),2021,15(01):1-3.
[3]Zheng X, Gao H, Zhang Y, Cui X, Jia R, Xue J, Tang W, Wang Y, Li H, Chen X, Wang H. Development of a rapid and sensitive UPLC-MS/MS assay for simultaneous quantitation of Vorolanib and its metabolite in human plasma and application to a pharmacokinetics study. J Pharm Biomed Anal. 2021 May 30;199:114034. doi: 10.1016/j.jpba.2021.114034. Epub 2021 Mar 22. PMID: 33774456.
[4] Sheng X, Yan X, Chi Z, Cui C, Si L, Tang B, Li S, Mao L, Lian B, Wang X, Bai X, Zhou L, Kong Y, Dai J, Ding L, Mao L, Guo J. Phase 1 trial of vorolanib (CM082) in combination with everolimus in patients with advanced clear-cell renal cell carcinoma. EBioMedicine. 2020 May;55:102755. doi: 10.1016/j.ebiom.2020.102755. Epub 2020 Apr 23. PMID: 32335374; PMCID: PMC7184160.
[5] Pedersen KS, Grierson PM, Picus J, Lockhart AC, Roth BJ, Liu J, Morton A, Chan E, Huffman J, Liang C, Wang-Gillam A, Tan B. Vorolanib (X-82), an oral anti-VEGFR/PDGFR/CSF1R tyrosine kinase inhibitor, with everolimus in solid tumors: results of a phase I study. Invest New Drugs. 2021 Oct;39(5):1298-1305. doi: 10.1007/s10637-021-01093-7. Epub 2021 Mar 18. PMID: 33738668.
[6] Chehrazi-Raffle A, Pal SK. Vorolanib and everolimus: Lenvatinib and everolimus part deux, or something new? EBioMedicine. 2020 Jun;56:102812. doi: 10.1016/j.ebiom.2020.102812. Epub 2020 Jun 5. PMID: 32512515; PMCID: PMC7276505.
[7] Liang C, Yuan X, Shen Z, Wang Y, Ding L. Vorolanib, a novel tyrosine receptor kinase receptor inhibitor with potent preclinical anti-angiogenic and anti-tumor activity. Mol Ther Oncolytics. 2022 Jan 10;24:577-584. doi: 10.1016/j.omto.2022.01.001. PMID: 35252556; PMCID: PMC8861424.
[8] Song Y, Wang J, Ren X, Jin J, Mao L, Liang C, Ding L, Yang L. Vorolanib, an oral VEGFR/PDGFR dual tyrosine kinase inhibitor for treatment of patients with advanced solid tumors: An open-label, phase I dose escalation and dose expansion trial. Chin J Cancer Res. 2021 Feb 28;33(1):103-114. doi: 10.21147/j.issn.1000-9604.2021.01.11. PMID: 33707933; PMCID: PMC7941683.

 京公网安备11010502042549号
京公网安备11010502042549号